Химические свойства кислот и оснований
В 11 задании продолжается тема химических свойств, на этот раз уже кислот и оснований.
Теория к заданию №11 ОГЭ по химии
Кислоты
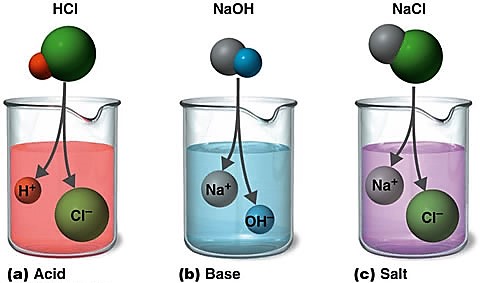
Напомню, что кислоты - это химические соединения, диссоциирующие на протоны (H+). Примеры простейших кислот - соляная (HCl), серная (H2SO4), азотная (HNO3).
Основания
Основания же - вещества, диссоциирующие на гидроксид ионы (OH-).
Простейшими примерами являются едкий калий и натрий (KOH и NaOH). Едкими их называют, кстати, неспроста. Они действительно разъедают и щиплют при попадании на кожу. Поэтому опасность их не стоит недооценивать.
Итак, перейдем к рассмотрению химических свойств данных классов.
Химические свойства кислот
Классификацию кислот мы рассматривали в разборе 5 задания ОГЭ по химии. Я рекомендую перед дальнейшем изучением химических свойств вспомнить классификацию кислот для общего понимания.
Итак, перейдем к рассмотрению свойств кислот:
- реакция с основными оксидами: в качестве примера приведена реакция оксида кальция с соляной кислотой. В данной реакции продуктами являются соль - хлорид кальция, которым посыпают дороги в гололёд, и вода, которую мы пьем каждый день.
- реакция с амфотерными оксидами, например оксидом цинка:
- реакция кислот со щелочами носит название нейтрализации. Как пример, приведена реакция едкого натра с соляной кислотой, продуктами являются соль (в данном примере поваренная) и вода.
- обменные реакции с солями, если в результате реакции образуется нерастворимое вещество либо газ. В качестве примера приведена реакция хлорида бария с серной кислотой, в результате которой образуется осадок сульфата бария и летучий хлороводород.
- реакция с нерастворимыми основаниями, например гидроксида меди с серной кислотой:
- вытеснение слабых кислот из растворов их солей, например солей фосфорной кислоты хлороводородной кислотой:
- реакция с металлами, стоящими в ряду напряжений до водорода - пример - реакция магния с соляной кислотой:
Химические свойства оснований
Перед изучением химических свойств оснований, полезно вспомнить классификацию оснований из 5 задания ОГЭ по химии.
Итак, перейдем к разбору химических свойств оснований:
- вышеприведенная реакция с кислотами - реакция нейтрализации
- реакция с амфотерными основаниями, например, гидроксидом цинка и алюминия:
- реакция с кислотными оксидами с образованием соли и воды. Пример - реакция едкого натрия с оксидом кремния (травление стекла):
- обменные реакции с солями, если образуется осадок или газ (аммиак). Пример - реакция гидроксида бария с сульфатом натрия:
Разбор типовых вариантов заданий ОГЭ по химии
Первый вариант задания
В реакцию с соляной кислотой вступает:
- нитрат серебра
- нитрат бария
- серебро
- оксид кремния
Рассмотрим каждый случай:
- Соляная кислота и нитрат серебра. Так как нитрат серебра - соль, обменная реакция возможна, если продукт реакции осадок либо газ. В качестве продукта может образоваться азотная кислота (растворима) и хлорид серебра (нерастворим - белый творожистый осадок). Значит, реакция возможна и ответ нам подходит.
- Нитрат бария и соляная кислота. Продукты данной реакции обмена растворимы (азотная кислота и хлорид бария), поэтому реакция не идет.
- Серебро стоит в ряду напряжений после водорода, поэтому не реагирует с кислотами-неокислителями.
- Оксид кремния - кислотный оксид и с кислотами не реагирует.
Ответ: 1



![{displaystyle {mathsf {Zn(OH)_{2}+2KOH {xrightarrow {}} K_{2}[Zn(OH)_{4}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/68e0f6384e8c3500423696be7e463304da768ec4)


Гидроксид калия реагирует с каждым из двух веществ
1)СаО и Р2О5
2)NaCl и H2
3)SO2 и H20
4)HCl и CO2
4
HCL и CO2
очень хороший и понятный разбор 11 задания в ОГЕ по химии, спасибо большое
реакция с амфотерными основаниями, например, гидроксидом цинка и алюминия:
ВОТ ТАМ ГИДРОКСИД ЦИНКА + едкинатор
Как узнать что в уравнении реакции выделился газ?