Химические свойства солей
Итак, начнем разбирать 12 задание из теста ОГЭ по химии на тему химические свойства средних солей.
Данное задание проще предыдущих. Если вы освоили решение 11 задания в ОГЭ по химии, то Вы с лёгкостью разберетесь с решением 12 задания.
Теория к заданию №12 ОГЭ по химии
Напомню, что соли - вещества образованные ионом металла и кислотным остатком:
Основная масса заданий основана на обменных реакциях, о которых я упоминал в химических свойствах кислот и оснований. Если в результате реакции образуется осадок, либо газ, либо вода - то реакция идет. Также соли реагируют с металлами, стоящими левее металла, входящего в состав соли - то есть более активного.
Разбор типовых вариантов задания №12 ОГЭ по химии
Первый вариант задания
Среди веществ: NaCl, Na2S, Na2SO4 – в реакцию с раствором Cu(NO3)2 вступает(-ют):
- только Na2S
- NaCl и Na2S
- Na2S и Na2SO4
- NaCl и Na2SO4
Для решения нам понадобится таблица растворимости:
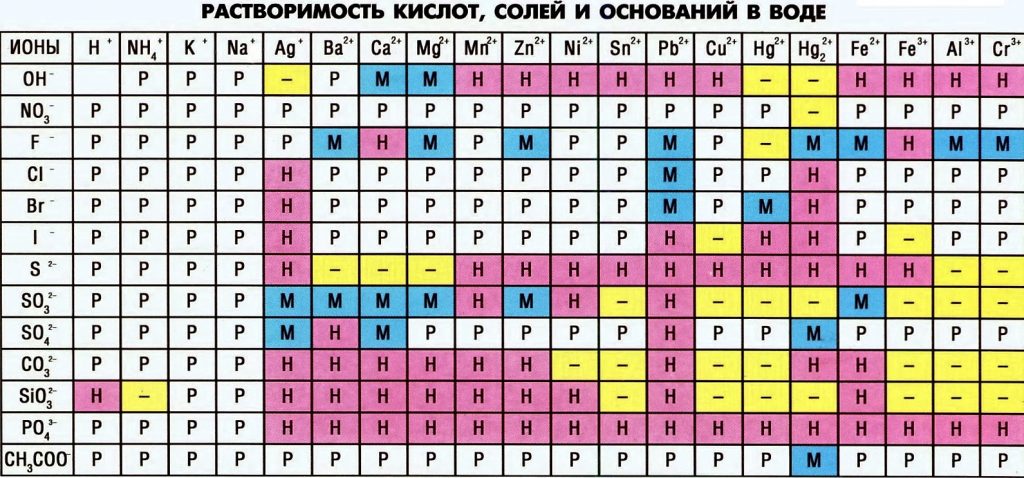
Посмотрим, как может прореагировать NaCl с нитратом меди:
NaCl + Cu(NO3)2 = 2 NaNO3 + Cu(Cl)2
Хлорид меди растворим, нитрат натрия тоже, значит данная реакция не идёт.
Рассмотрим реакцию сульфида натрия с нитратом меди:
Na2S + Cu(NO3)2 = 2 NaNO3 + CuS
Нитрат натрия растворим, а сульфид меди - осадок, поэтому реакция идет.
Сульфат натрия с нитратом меди:
Na2SO4 + Cu(NO3)2 = 2 NaNO3 + CuSO4
Сульфат меди растворим, а значит реакция не идет.
Выбираем правильный ответ - 1.
Ответ: 1
спасибо большое, очень помогли! <3
Спасибо большое, всё очень понятно)
ответ — 3 т.к CuSo4 нерастворимая соль
в каком месте она нерастворимая?
вы ошибаетесь CuSo4 растворимая соль.
Очень мало вариантов заданий,не все задания могу решать из ОГЭ,берите несколько абсолютно разных вариантов и объясняйте каждый, и ваш сайт станет намного лучше ?