Задание №12 ЕГЭ по физике
Первичный бал: 1 Сложность (от 1 до 3): 1 Среднее время выполнения: 1 мин.
Задание №12 в ЕГЭ по физике - последнее тестовое задание на тему термодинамики.
Задание ЕГЭ-Ф-ДВ2023-10
- При температуре 23°С влажность воздуха в сосуде была равна 48,5%.
- В течение всего опыта в сосуде находилась вода в жидком состоянии.
- Так как объём сосуда не изменялся, давление влажного воздуха увеличивалось пропорционально его температуре.
- В начальном состоянии при температуре 289 К пар в сосуде был насыщенный.
- Парциальное давление сухого воздуха в сосуде не изменялось.
Алгоритм решения:
- Проверить истинность утверждения 1. Для этого необходимо определить влажность воздуха в сосуде при температуре 23°С и сравнить ее с предложенным значением.
- Проверить истинность утверждения 2. Для этого необходимо установить, испарилась ли вся вода к концу опыту, или часть ее осталась жидкой.
- Проверить истинность утверждения 3. Для этого необходимо записать формулу, отображающую зависимость между давлением насыщенного пара, его объемом, плотностью и температурой.
- Проверить истинность утверждения 4. Для этого нужно определить влажность воздуха в начале опыта.
- Проверить истинность утверждения 5. Для этого необходимо установить, как изменялось парциальное давление сухого воздуха в течение всего опыта.
- Записать ответ в виде последовательности цифр, не разделенных знаками препинания и пробелами.
Решение:
Проверяем истинность утверждения 1, согласно которому при температуре 23°С влажность воздуха в сосуде была равна 48,5%. Чтобы доказать или опровергнуть утверждение, поразмыслим о том, что происходило в сосуде все это время.
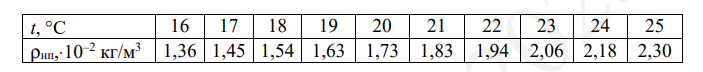
Сосуд изначально длительное время находился при температуре 289 К, что соответствует 16 градусам Цельсия. При этом внутри него был влажный воздух и вода массой 10 г. Так как количество воды не менялось, делаем вывод, что система находилась в динамическом равновесии — количество испаренных молекул было равно количеству молекул, вернувшихся в жидкость. Значит, изначально в сосуде пар был насыщенным.
Плотность насыщенных паров при 16 °С равна 1,36∙10–2 кг/м3. Это значит, что влажный воздух содержал 13,6 грамм испаренной воды. Еще 10 грамм оставались в сосуде в жидком состоянии.
Когда сосуд начали медленно нагревать, постепенно начала испаряться вода. При этом количество воды уменьшалось, а пар все равно оставался насыщенным до тех пор, пока не испарилась вся вода. Необходимо проверить, испарилась ли она в момент, когда температура достигла 23°С. Плотность насыщенных паров в это время была равна 2,06∙10–2 кг/м3. Значит, влажный воздух содержал 20,6 грамм испаренной воды. Это всего на 7 грамм больше по сравнению с начальным моментом времени. Значит, вода еще испарилась не полностью — в количестве 3 грамм она находилась в жидком состоянии. Следовательно, при температуре 23°С влажность воздуха была равна 100%. Утверждение 1 неверно.
Проверяем истинность утверждения 2, согласно которому в течение всего опыта в сосуде находилась вода в жидком состоянии. Чтобы проверить это, нужно понять, испарилась ли вся вода к концу опыта, или нет. Плотность насыщенного пара в конце опыта, когда температуры была равна 25°С, составляла 2,3∙10–2 кг/м3. Значит, влажный воздух содержал 23 грамма воды. Изначально в нем было 13,6 грамм. Значит, испарилось еще 9,4 грамма. А 0,6 грамма воды остались в сосуде жидкими. Следовательно, утверждение 2 верно.
Проверяем истинность утверждения 3, согласно которому давление влажного воздуха увеличивалось пропорционально его температуре, так как объем сосуда не изменялся.
Применим уравнение состояния идеального газа:
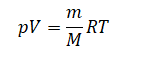
Перенесем давление в правую часть уравнения:
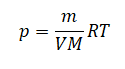
Отношение массы к объему есть плотность. Следовательно:
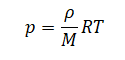
С нагреванием сосуда увеличивается не только температура, но и плотность насыщенного пара. А потому давление влажного воздуха увеличивалось пропорционально произведению плотности насыщенных паров на температуру. Следовательно, утверждение 3 неверно.
Проверяем истинность утверждения 4, согласно которому в начальном состоянии при температуре 289 К пар в сосуде был насыщенный. Проверяя утверждение 1, мы уже пришли к этому выводу. Следовательно, утверждение 4 верно.
Проверяем истинность утверждения 5, согласно которому парциальное давление сухого воздуха в сосуде не изменялось. Это неверно, так как при постоянном объеме и постоянной массе с увеличением температуры давление увеличивается.
Следовательно, ответом является последовательность цифр 24.
Ответ: 24pазбирался: Алиса Никитина | обсудить разбор
Задание EF22749
 Одноатомный идеальный газ в количестве ν моль помещают в открытый сверху сосуд под лёгкий подвижный поршень и начинают нагревать. Начальный объём газа V0, давление p0. Масса газа в сосуде остаётся неизменной. Трением между поршнем и стенками сосуда пренебречь. R– универсальная газовая постоянная.
Одноатомный идеальный газ в количестве ν моль помещают в открытый сверху сосуд под лёгкий подвижный поршень и начинают нагревать. Начальный объём газа V0, давление p0. Масса газа в сосуде остаётся неизменной. Трением между поршнем и стенками сосуда пренебречь. R– универсальная газовая постоянная.
Установите соответствие между физическими величинами, характеризующими газ, и формулами, выражающими их зависимость от абсолютной температуры T газа в условиях данной задачи.
К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
Алгоритм решения
Решение
Уравнение состояния идеального газа имеет вид:
pV=mMRT
Учтем, что отношение массы к молярной массе есть количество вещества.Отсюда объем равен:
V=νRTp
Следовательно, первой цифрой ответа будет «1».
Внутренняя энергия идеального газа равна сумме кинетических энергий всех молекул этого газа:
E=N−Ek
Запишем основное уравнение МКТ:
p=nkT
Отсюда температура газа равна:
T=pnk
Но температура прямо пропорциональна средней кинетической энергии молекул газа:
T=2−Ek3k
Следовательно:
pnk=2−Ek3k
−Ek=3p2n
E=N−Ek=N3p2n
Но концентрация определяется отношением количества молекул к объему. Следовательно:
E=N3pV2N=3pV2
А произведение давления на объем можно выразить через уравнение Менделеева — Клапейрона. Следовательно:
E=32νRT
Вторая цифра ответа будет «3».
Ответ: 13pазбирался: Алиса Никитина | обсудить разбор
Задание EF17664
Зависимость объёма идеального газа от температуры показана на VТ-диаграмме (см. рисунок). В какой из точек давление газа максимально? Масса газа постоянна.
Ответ:
A
B
C
D
Алгоритм решения
Решение
Запишем уравнение состояния идеального газа:
pV=νRT
Отсюда видно, что давление прямо пропорционально температуре. Это значит, что с ростом температуры давление увеличивается.
Также видно, что давление обратно пропорционально объему. Следовательно, давление увеличивается с уменьшением объема.
Отсюда следует, что давление будет максимальным в той точке, в которой температура максимальна, а объем минимален. Такой точкой является точка D.
Ответ: Dpазбирался: Алиса Никитина | обсудить разбор
Задание EF18873
 В сосуде неизменного объёма при комнатной температуре находилась смесь неона и аргона, по 1 моль каждого. Половину содержимого сосуда выпустили, а затем добавили в сосуд 1 моль аргона. Как изменились в результате парциальное давление неона и давление смеси газов, если температура газов в сосуде поддерживалась неизменной?
В сосуде неизменного объёма при комнатной температуре находилась смесь неона и аргона, по 1 моль каждого. Половину содержимого сосуда выпустили, а затем добавили в сосуд 1 моль аргона. Как изменились в результате парциальное давление неона и давление смеси газов, если температура газов в сосуде поддерживалась неизменной?
Для каждой величины определите соответствующий характер изменения:
- увеличилась
- уменьшилась
- не изменилась
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Алгоритм решения
Решение
Исходные данные:
Сначала парциальное давление неона и аргона равно. Это объясняется тем, что давление газов при неизменном количестве вещества зависит только от объема и температуры. Эти величины постоянны.
Когда из сосуда выпустили половину газовой смеси, в нем оказалось по половине моля каждого из газов. Затем в сосуд впустили 1 моль аргона. Следовательно, в сосуде стало содержаться 0,5 моль неона и 1,5 моль аргона. Запишем уравнение Менделеева — Клапейрона:
pV=νRT
Из уравнения видно, что давление и количество вещества — прямо пропорциональные величины. Следовательно, если количество неона уменьшилось, то его парциальное давление тоже уменьшилось.
Общая сумма количества вещества равна сумме количеств вещества 1 (неона) и 2 (аргона): 0,5 + 1,5 = 2 (моль). Изначально в сосуде тоже содержалось 2 моль газа. Так как количество вещества, температура и объем сохранились, давление тоже осталось неизменным.
Ответ: 23pазбирался: Алиса Никитина | обсудить разбор
Задание EF17701
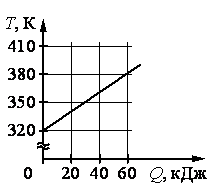 На рисунке изображён график зависимости температуры тела от подводимого к нему количества теплоты. Удельная теплоёмкость вещества этого тела равна 500 Дж/(кг⋅К). Чему равна масса тела?
На рисунке изображён график зависимости температуры тела от подводимого к нему количества теплоты. Удельная теплоёмкость вещества этого тела равна 500 Дж/(кг⋅К). Чему равна масса тела?
Ответ:
а) 1 кг
б) 2 кг
в) 3 кг
г) 4 кг
Алгоритм решения
Решение
Запишем исходные данные и те данные, что получится выделить из графика:
60 кДж = 60∙103 Дж
Количество теплоты вычисляется по формуле:
Q=cm(t−t0)
Отсюда масса вещества равна:
m=Qc(t−t0)=60·103500(380−320)=2 (кг)
Ответ: бpазбирался: Алиса Никитина | обсудить разбор
Задание EF18295
Температура нагревателя идеального теплового двигателя, работающего по циклу Карно, равна T1, а температура холодильника равна T2. За цикл двигатель получает от нагревателя количество теплоты Q1. Установите соответствие между физическими величинами и формулами, по которым их можно рассчитать.
К каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами.

Алгоритм решения
Решение
КПД двигателя определяется отношением разности температур нагревателя и холодильника к температуре нагревателя:
η=T1−T2T1=1−T2T1
Верный ответ для «А» — 1.
Работа, совершаемая за цикл, определяется произведением КПД на количество теплоты, полученного от нагревателя:
A=Qη=Q(T1−T2T1)
Верный ответ для «Б» — 2.
Ответ: 12
pазбирался: Алиса Никитина | обсудить разбор
👀 8.1k